中國虎網 2016/3/10 0:00:00 來源:
未知
國家藥監總局3月9日發布《化學
藥品注冊分類改革工作方案的公告》,本文通過
國務院同意,這表明藥品注冊分類工作已推向國家戰略高度。
此次全新的注冊分類辦法從六類縮減成五類,更讓人關注的是,“臨床療效”的概念更加強烈,“改良型新藥要求比改良前具有明顯的臨床優勢”、"仿制藥與原研藥品質量和療效一致"的字眼在《公告》中更加明顯,這也就意味著治療效果將成為檢驗新藥質量最重要的指標。
該《公告》的出臺,預示著我國藥品注冊工作的又一個里程碑,而對于制藥行業來說,在苦苦掙扎了半年許久之后,藥品注冊申請工作又能"有法可依"而繼續進行。那么,新版藥品注冊分類改革將會產業帶來哪些變化呢?
重啟藥品注冊工作
自從去年藥品7月22日,藥監部門開始臨床試驗自查、核查,不僅僅改變了研發生態、藥品競爭格局、新品上市節奏。
《公告》的出臺解決了藥品注冊申報資料的方向問題,明確了自己的資料需要什么,如不滿足要求該如何補充資料,讓注冊資料的撰寫工作重新啟動起來,注冊工作得以繼續運轉。
但對于對中小企業來講,更是挑戰。他們如果沒有創新能力與資金來源,要盡早謀求兼并。有分析人士指出,轉行也是企業可以考慮的,利用現有的條件和設備做化工品等。而大企業則應該繼續走新藥研發的道路,以占據一定的市場地位。
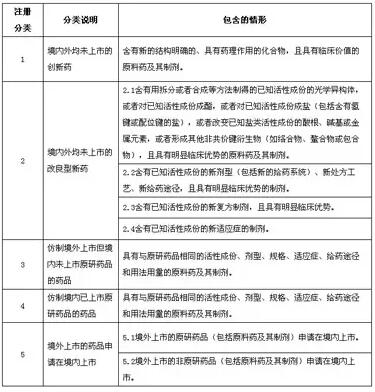
(圖為化學藥品新注冊分類、說明及包含的情形)
與全球逐漸接軌
境內外均未上市的創新藥可進行申報是此次注冊分類的最大看點。
眾所周知,我國的藥品分類注冊辦法一直相對于保守,普遍是在經歷過歐美藥監部門審批之后,才能在中國進行申報,大大延緩了專利藥的上市時間。
而這一條目的修改將使中國享受到重磅藥物全球同步上市的政策紅利,這對中國藥品開發和質量提升,以及新藥的研發有很好的促進作用。但具體如何申報注冊,業內還存有疑問。
國內的制藥企業今后在研發新藥時,首先要考慮臨床需求,其次是藥物在上市后是否還有改進的空間。有分析人士指出,我們對手已不局限于國內市場了,與全球發達國家接軌已實在必行。
藥品上市許可人
"藥品上市許可人制度"是將上市許可與生產許可實行分離管理的制度模式,使得藥品上市許可與生產企業不再捆綁,美國、歐盟各國以及日本等國家均實行該制度,而我國,目前已經開始了試點工作。
新的化藥分類,是上市許可持有人制度及新藥審批改革中重要的一環,"上市許可人"作為藥品研發的責任主體需與藥品注冊要求相協調,只有將上市許可與注冊分類規定的明確之后,方能為更為細致的政策和概念的出臺打下基礎。
《公告》中對不同類型的藥品相對應的上市許可人的任務進行了劃分,這樣更有利于"許可人"的研發方向。
網站聲明:
1、本網部分資訊為網上搜集轉載,為網友學習交流之用,不做其它商業用途,且均盡最大努力標明作者和出處。對于本網刊載作品涉及版權等問題的,請作者第一時間與本網站聯系,聯系郵箱:tignet@vip.163.com 本網站核實確認后會盡快予以妥當處理。對于本網轉載作品,并不意味著認同該作品的觀點或真實性。如其他媒體、網站或個人轉載使用,請與著作權人聯系,并自負法律責任。
2、凡本網注明"來源:虎網"的所有作品,版權均屬虎網所有,未經本網授權不得轉載、鏈接、轉貼或以其他方式使用;已經本網授權的,應在授權范圍內使用,且必須注明"來源:虎網"。違反上述聲明者,本網將追究其法律責任。